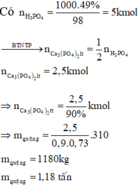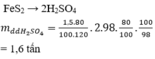Từ quặng photphorit, có thể điều chế axit photphoric theo sơ đồ sau:
![]()
Biết hiệu suất chung của cả quá trình là 90%. Để điều chế được 1 tấn dung dịch H3PO4 49%, cần bao nhiêu tấn quặng photphorit chứa 73% Ca3(PO4)2 về khối lượng?
A. 1,32tấn
B. 1,23tấn
C. 1,81tấn
D. 1,18tấn